Presentasi 3: Reaksi Senyawa Organologam (Analisis Kondisi dan Produk)
- April 01, 2018
- By HANA
- 3 Comments
Pengantar
Pereaksi
organologam adalah senyawa yang mengandung ikatan karbon-logam. Untuk keperluan diskusi kali ini,
satu-satunya senyawa yang akan kita pertimbangkan adalah yang mana M = Li atau
Mg. Ketika M = Li, reagen organologam disebut reagen organolithium. Ketika M =
Mg, itu disebut pereaksi Grignard. Secara historis, pereaksi Grignard
dikembangkan sebelum reagen organolithium. Namun, dalam beberapa tahun
terakhir, reagen organolithium telah mengambil alih peran kunci yang digunakan
reagen Grignard sebagai sumber karbon nukleofilik paling serbaguna.
Karakter
nukleofilik dari reagen organologam berasal dari fakta bahwa ikatan C-M
terpolarisasi sedemikian rupa sehingga atom karbon negatif sementara atom logam
positif.
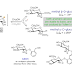
Seperti yang ditunjukkan gambar
di atas, ikatan karbon-logam memiliki "karakter ionik". Bahkan,
penting untuk berpikir tentang pereaksi Grignard dan reagen organolithium
sebagai sumber atom karbon bermuatan negatif, yaitu karbanion. Karena karbon
bukanlah unsur yang sangat elektronegatif, karbon sangat reaktif ketika
mengandung muatan negatif.
Persiapan
Karena organologam sangat
reaktif, reagen organologam umumnya disiapkan tepat sebelum digunakan.
Organolithium reagen tersedia secara komersial sebagai solusi dalam pelarut
inert seperti dietil eter, tetrahidrofuran (THF), atau pentana. Namun, mereka
memiliki umur simpan yang pendek dan harus ditangani di bawah atmosfer inert.
Prosedur untuk menghasilkan tipe reagen serupa: alkil atau aril halida
diperlakukan dengan magnesium atau logam litium dalam pelarut kering, inert,
eter anhidrat yang paling umum. Persamaan 1 dan 2 menggambarkan persiapan fenil
magnesium bromida dan metil litium, masing-masing.
Reaksi
1. Organometallic Reagen sebagai
Basa
Organologam seperti fenilmagnesium bromida dan metil lithium adalah salah satu basa
terkuat yang ada. Akibatnya mereka akan mendeprotonasikan senyawa seperti
amina, alkohol, dan asam karboksilat. Gambar 2 menyajikan satu reaksi yang
mewakili masing-masing situasi ini.
Reaksi Asam-Basa Reagen
Organometalik
Konstanta kesetimbangan untuk
masing-masing reaksi ini sangat besar. Reaksi-reaksi ini semua terjadi sangat cepat,
kadang-kadang eksplosif. Reaktivitas ekstrim reagen organologam terhadap
kelompok O-H dan N-H umumnya membuat kelompok-kelompok ini tidak dapat
digunakan jika Anda ingin memanfaatkan reagen organologam sebagai nukleofil.
2. Organometallic Reagen sebagai
Nukleofil
Apakah suatu reagen organologam
diklasifikasikan sebagai basa atau nukleofil bergantung pada apakah ia
membentuk ikatan dengan atom hidrogen atau atom karbon. Jika reaktan mengandung
karbon elektrofilik dan tidak mengandung gugus O-H atau N-H, maka reagen
organologam akan bertindak sebagai nukleofil terhadap atom karbon elektrofilik
tersebut. Sumber karbon elektrofil yang paling umum adalah gugus karbonil,
terutama gugus karbonil aldehid dan keton.
Persamaan 3 dan 4 menggambarkan
reaktivitas nukleofilik fenilmagnesium bromida dan metil litium terhadap aldehid
sederhana dan keton sederhana.
Seperti persamaan ini menekankan,
masing-masing reaksi ini mengarah pada pembentukan ikatan C-C. Ini adalah dasar
kimia organik sintetis.Prinsip fundamental yang memandu pengembangan pendekatan
logis untuk persiapan molekul baru adalah pembentukan ikatan karbon-karbon
membutuhkan interaksi molekul yang mengandung atom karbon dari polaritas yang
berlawanan. Kita telah melihat bahwa ikatan C-O dalam gugus karbonil memiliki
dipol ikatan dengan atom karbon yang kekurangan elektron.
Dalam Persamaan 4 karbon karbonil
dari propiophenone disorot dengan
warna hitam untuk menekankan karakter elektrofiliknya, sementara sifat
nukleofilik karbon dalam metil litium
ditekankan dengan mewarnainya merah.
Mekanisme Reaksi
Reaksi reagen organologam dengan aldehida
atau keton merupakan reaksi paling mendasar dari gugus karbonil: penambahan
nukleofilik. Mekanisme reaksi melibatkan dua langkah:
1. penambahan reagen organologam
ke karbon karbonil untuk membentuk tetrahedral intermediate
2. protonasi ion alkoksida yang
dihasilkan.
Gambar berikut merangkum dua
langkah diatas.
Mekanisme Penambahan Nukleofilik
pada Kelompok Karbonil
Permasalahan
1. Apa maksud pereaksi
organologam digunakan in-situ ?
2. Apa keistimewaan organologam
sehingga dapat dimanfaatkan sebagai pereaksi pembentukan Alkohol?
3. Bagaimana karbon bisa
bermuatan negative menjadi karbanion?













3 komentar
Saya akan menjawab pertanyaan kedua hal tersebut dapat terjadi karena logam sangat bersifat elektropositif. Sehingga karena adanya carbon dan juga logam yang mana keduanya memiliki gaya dipol-dipol yang sama-sama bermuatan positif yang mana terjadi tolak menolak kemudian karena elektron yang terus bergerak akan menyebabkan terjadinya tumbukan sehingga salah satu yang bermuatan positif terjadi perubahan menjadi negatif yang mana hal ini terjadi pada karbon yang sebelumnya bermuatan positif menjadi bermuatan negatif
BalasHapusSaya akan menjawab pertanyaan ketiga yaitu Bagaimana karbon bisa bermuatan negative menjadi karbanion?
BalasHapusJawabannya karena Hal tersebut dikarenakan karbon dalam senyawa organologam terikat pada suatu unsur elektropositif yang berarti karbon tersebut akan berfungsi sebagai basa atau nukleofil dan karena itu karbon tersebut bermuatan negatif.
Assalamualaikun wr, wb, saya Maya Rizkita (A1C116028) akan mennawab pertanyaan pertama (1),
BalasHapusDilakukan in situ karena organologam sangat reaktif terhadap oksigen dan berlangsung sangat cepat. Maka dilakukan dalam kondisi bebas oksigen. Semoga bermanfaat.